
2024年3月,ICH管理委员会决定成立S13:寡核苷酸疗法的非临床安全性研究专家工作组。海昶生物资深副总裁兼核酸创新研究院院长杨永胜博士凭借丰富的行业经验、深厚的学术背景以及在核酸药物研发领域的杰出成就,经中国医药创新促进会筛选推荐,国际药品制造商协会联合会(IFPMA)审核确认,成功入选IFPMA ICH S13专家工作组。
入选名单:
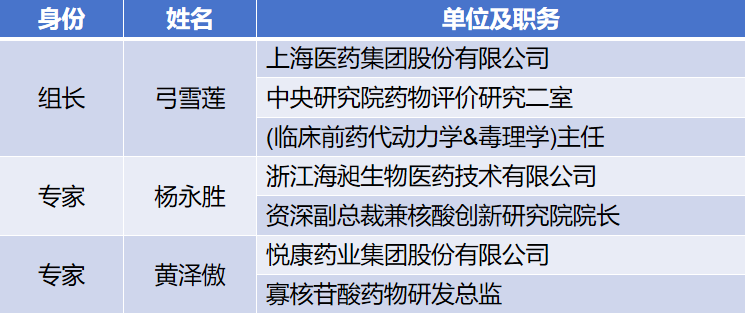
展望未来,杨永胜博士将与另外两位中国专家携手并进,深度参与S13指导原则的起草、修订工作,积极促进国际间合作与交流,共同推动ICH指导原则在全球范围内的广泛应用与持续优化,为全球医药健康事业的进步贡献中国智慧与力量。
专家简介

杨永胜博士,专注于ASO、siRNA、miRNA和mRNA等核酸药物的研发和临床转化,2022年10月,mRNA疫苗项目获得美国IND批件。曾在美国FDA工作16年,任资深药理学家,负责新药和仿制药的生物药剂学和药品质量的研究和评价,对仿制药包括复杂制剂如脂质体、微球和局部作用药物的生物等效性研究结果进行审评在密西根大学期间,主要从事基因治疗方面的研究工作,利用GalNAc成分作为基因的递送系统,以便靶向性地作用于肝细胞。对质粒的制备,DNA的放射性标记,递送系统的构建,制剂处方和工艺的筛选和优化,制剂的主要理化特征如粒径分布和表面电荷的分析评估,体内外的基因表达,以及体内组织分布和药物代谢动力学,进行了深入系统的研究,积累了丰富的经验。曾在国内率先开展新型药物递送系统脂质体的研究,包括处方和工艺的筛选和优化,主要理化特征的分析评估,以及安全性、有效性和药物代谢动力学的研究。发表研究论文50余篇,参编著作多部,获美国专利1项,多次获得美国人类健康服务部和FDA的奖励。
关于海昶生物:
浙江海昶生物医药技术有限公司位于杭州市中国医药港,是一家以生物医药技术创新开发业务为主营,具有自主创新能力和全球知识产权布局的国家高新技术企业。公司紧紧围绕“分享、进取、求真、务实”的核心价值观,以药物递送系统开发和产业化为核心,专注于小核酸药物、mRNA疫苗等核酸创新药及复杂注射剂的开发。目前,白蛋白紫杉醇已在中国及欧盟获批上市,一带一路多个国家注册申报中;小核酸I类新药HC0301已获FDA和NMPA双重批准,正开展全球多中心II期临床试验;mRNA新冠疫苗加强针获FDA批准临床,为国内首支获得美国临床批件的mRNA疫苗产品。产品管线覆盖传染病预防、肿瘤免疫治疗、抗肿瘤、镇痛等领域。